Peptidähnliche Synthese-Technologie
Die Forschung und Entwicklung von Peptidmedikamenten wächst in der Medizin schnell. Die Entwicklung von Peptidmedikamenten ist jedoch durch ihre eigenen Merkmale begrenzt. Beispielsweise wird aufgrund der besonderen Empfindlichkeit gegenüber enzymatischer Hydrolyse die Stabilität verringert, und die Variabilität der sterischen Konformation führt zu einer geringen Zielspezifität, einer geringen Hydrophobie und dem Fehlen eines spezifischen Transportsystems. Um diese Peptide zu überwinden, ist eine von ihnen vorgeschlagene Lösungen und eine erfolgreiche Anwendung einer Art von Peptid.
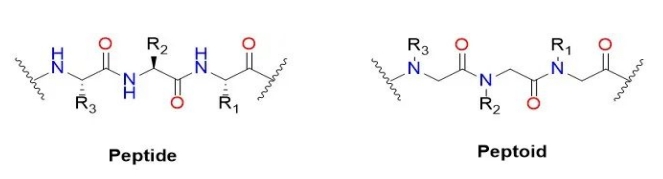
Art von Peptid (englischer Name: Peptoid) oder Poly - N - anstelle von Glycin (englischer Name: Poly Real - N - Substituiertes Glycin), ist es ein quasi -Peptidverbindungen von Peptid in der Hauptkette. Die Alpha -Kohlenstoff -Seitenkette überträgt den Hauptkettenstickstoff anstelle der Seitenkette. Im ursprünglichen Polypeptid repräsentiert die R -Gruppe der Aminosäure -Seitenkette 20 verschiedene Aminosäuren, aber die R -Gruppe hat mehr Optionen im Peptoid. Im Peptid Peptid auf der Hauptkette von Aminosäuren in Alpha -Kohlenstoffstickstoff anstelle der Seitenkette -Transfer in die Hauptkette. Erwähnenswert ist erwähnenswert, dass Peptide im Allgemeinen nicht die gleichen hochrangigen geordneten Strukturen wie Sekundärstrukturen in Peptiden und Proteinen aufgrund des Mangels an Wasserstoff am Stickstoff des Rückgrats produzieren. Peptid -Anfangszweck besteht darin, ein stabiles und Proteasepeptid von kleinen Molekülenmedikamenten zu entwickeln.
Analyse von peptidähnlichen Synthese-Techniken
Die Methode der Peptidsynthese wurde eingeführt
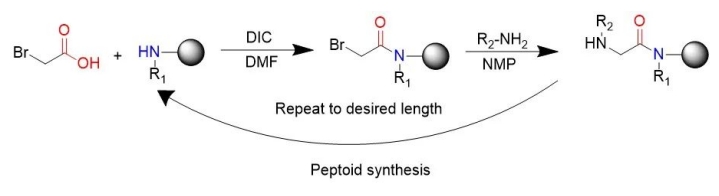
Die allgemein beliebte peptidartige Synthesemethode ist die von Ronzuckermann erfundene Subsingle-Synthesemethode, die jeweils in zwei Schritte unterteilt ist: Acylierung und Verschiebung. In der Acylierung besteht der erste Schritt darin, die Halozisesäure so zu aktivieren, dass die Amine am Ende des vorherigen Schritts verbleiben, am häufigsten diisopropylkarbonisiertes Diimin. Bromoätikum wurde durch Diisopropylcarbodiimid aktiviert. "Bei Substitutionsreaktionen (bimolekulare nukleophile Substitutionsreaktionen), ein Amin, typischerweise primär, greift das alternative Halogen an, um einen n-substituierten Glycin zu bilden." Der synthetische Untergrabungsweg verwendet leicht verfügbare primäre Amine, um Peptide zu erzeugen, wodurch die chemische Synthese von Peptiden ermöglicht wird.
Solide Erweiterung in den Klassenpeptiden -Synthese hat die reichhaltige Erfahrung und kann Ihnen eine Vielzahl von Peptid -Synthese -Service bieten.
Analyse von peptidähnlichen Synthese-Techniken
Der Vorteil eines solchen Peptids
Stabiler: Peptoide sind in vivo stabiler als Peptide.
Mehr Selektivität: Peptoide eignen sich gut für kombinierte Arzneimittelentdeckungsstudien, da eine Vielzahl verschiedener Polypeptidbausteine durch Modifikation der Backbone -Amino -Gruppe erhalten werden kann.
Effizienter: Die Häufigkeit von Peptoidstrukturen kann Peptoid zu einer guten Wahl für die Scan -Methodik machen, um schnell spezifische Strukturen zu finden, die an Proteine binden.
Mehr Marktpotential: Die Merkmale der Art von Peptid lassen es zu einer Art Arzneimittelentwicklung werden ein großes Potenzial.
Postzeit: 2025-07-02