Was sind Aminosäuren?
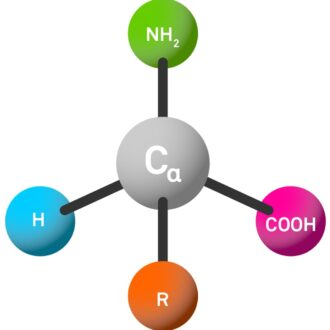
Die häufigsten Aminosäuren in der Natur werden als α-Aminosäuren bezeichnet. Diese Moleküle haben vier verschiedene Substituenten, die am zentralen Kohlenstoffatom (als α-C-Atom bezeichnet) gebunden sind:
Amino (NH₂, Drei-Buchstaben-Code als "H-" abgekürzt).
Carboxylsäuregruppe (Cooh, im Drei-Buchstaben-Code als "-Oh" abgekürzt).
Seitenketten(R, die sehr variabel sind und die Eigenschaften von Aminosäuren sowie das endgültige Peptid bestimmen).
Wasserstoffatom (H).
Die Verbindung von α-C-Atomen zu diesen vier verschiedenen Gruppen ergibt einzigartige chemische Eigenschaften, die eine Schlüsselrolle bei der Bestimmung des Verhaltens und der Eigenschaften von Aminosäuren und Peptiden spielen.
Biologische Aktivität von Aminosäuren
Aminosäuren können biologische Aktivitäten aufweisen wie:
Tryptophan (TRP) und Glutaminsäure (GLU) spielen eine Schlüsselrolle bei metabolischen Prozessen.
Die R -Gruppe (oder Seitenkette) bestimmt die einzigartigen Eigenschaften von Aminosäuren. Diese Gruppen können:
In einfachen Worten:Ein Wasserstoffatom wie Glycin (Gly).
Andere Säuren sind enthalten: wie Asparaginsäure (ASP) und Glutaminsäure (GLU).
Basisgruppen tragen:Arginin (Arg), Lysin (Lys) oder Histidin (His).
Enthält polare Gruppen: wie Serin (Ser) oder Threonin (Thr).
Nichtpolare Kohlenwasserstoffe:Alanin (Ala), Phenylalanin (Phe) oder Valin (Val).
Schwefelgehalt:wie in Cystein (Cys) und Methionin (Met) zu sehen.
Die Rolle von L-Aminosäuren und D-Aminosäuren
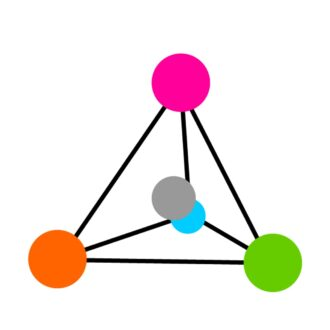
Die vier Substituenten des α-C-Atoms sind an den Ecken des Tetraeders mit dem α-C-Atom in der Mitte angeordnet (siehe Abbildung 3). Diese Anordnung ermöglicht es den beiden Formen von Aminosäuremolekülen in Spiegelform, ähnlich wie die linken und rechten Hände. Diese Spiegelformen werden als "Stereoisomere" oder "Enantiomere" bezeichnet.
Biologische Bedeutung von Enantiomeren
Obwohl Enantiomere nahezu identische chemische und physikalische Eigenschaften aufweisen, können sich ihre biologischen Wirkungen erheblich unterscheiden. Die molekulare Form ist für die Wechselwirkung mit biologischen Zielen von entscheidender Bedeutung. Ein Enantiomer kann effektiv an das Ziel binden, ein anderer kann nicht oder in einigen Fällen eine negative Wirkung haben. In Lösung dreht das Enantiomer die polarisierte Lichtebene in die entgegengesetzte Richtung.
Postzeit: 2025-09-05
